ТЕЛОМЕРЫ И ТЕЛОМЕРАЗА
В дни сенсационных сообщений в прессе — о чуть ли не открытии
пути бессмертия для всего человечества — в Институте цитологии и
генетики состоялся семинар, на котором основной доклад сделал
член-корреспондент РАН Игорь Жимулев. Уже пять лет он читает в
НГУ в рамках своего курса лекцию, которая так и называется
"Теломераза". Пожалуй, Игорь Федорович — один из самых
информированных в стране людей по поводу теломеразы, истории ее
изучения и сопутствующих тому исследований. Редакция "НВС"
попросила его внести ясность в это широкомасштабное
"всегосударственное" обсуждение, главенствующая роль в котором
оказалась отданной журналистам, а не специалистам.
И.Жимулев,
член-корреспондент РАН, зав.лабораторией молекулярной
цитогенетики Института цитологии и генетики СО РАН.
16 января 1998 года в американском журнале Science (том 279, N5349,
стр.349-352) появилась статья, авторы которой сообщили об
успешном эксперименте, позволившем увеличить продолжительность
жизни клеток, в пробирке или, как говорят биологи, in vitro.
Об этих результатах сообщили фактически все информационные
агентства.
Несмотря на то, что сами авторы оценили свои результаты
достаточно скромно, заявив всего лишь, что "способность
поддерживать клетки человека в юном состоянии может иметь
применение в исследованиях и медицине", научные популяризаторы и
журналисты уже начали обсуждать возможности принимать таблетки от
старости как аспирин.
Что же такое теломера, и как она может повлиять на
продолжительность жизни?
Известно, что гены живых существ расположены в хромосомах —
длинных высокополимерных молекулах дезоксирибонуклеиновой кислоты
- ДНК. Фрагмент ДНК, достигающий длины нескольких сантиметров, в
комплексе с молекулами многочисленных белков и составляет
хромосому.
В 1932 году один из основоположников генетики Нобелевский лауреат
Герман Мёллер обратил внимание на особое поведение концевых
участков хромосом после облучения рентгеновскими лучами. Он
предположил, что существуют особые структуры как бы
"запечатывающие" концы хромосом и предотвращающие их склеивание
друг с другом. Он назвал их "теломерами", т.е. в переводе с
греческого, — "концевыми частичками".
После открытия в 1953 году молекулярной структуры ДНК Д.Уотсоном
и Ф.Криком перед молекулярными биологами встал вопрос о механизме
завершения размножения (или репликации) ДНК на самых концах
молекулы. Известно, что молекула ДНК имеет двуцепочечное
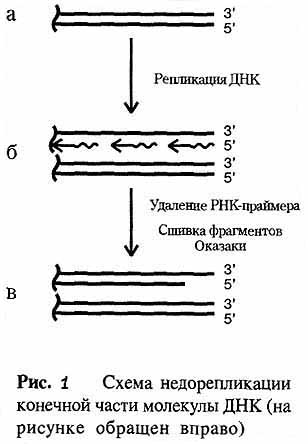
строение. В процессе репликации цепи расходятся (см. рис. 1). На
одной из них строится новая непрерывная комплементарная цепь, в
результате чего восстанавливается исходная двуцепочечная
структура. Процедура синтеза ДНК на второй из разошедшихся цепей
значительно сложнее: она строится из кусочков. Сначала
синтезируются короткие фрагменты РНК, так называемые затравки
(или праймеры). Они показаны волнистыми линиями на рис. 1. На
3'-концах этих праймеров синтезируются участки цепи ДНК —
фрагменты Оказаки (линии со стрелками на рис. 1). Затем праймеры
РНК разрушаются, и получившиеся бреши достраиваются. При этом, в
качестве праймеров используются 3'-концы фрагментов Оказаки.
Нетрудно заметить (рис. 1), что на самом конце одной из 4 цепей
ДНК образовалась брешь, т.к. на конце хромосомы попросту нет
фрагмента Оказаки, который бы можно было использовать в качестве
затравки.
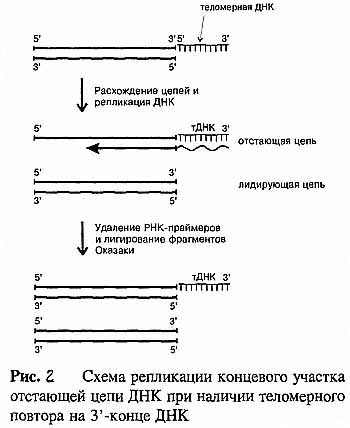 Эту проблему завершения репликации на концах линейных молекул ДНК
блестяще разобрал и решил российский ученый А.Оловников, ныне
сотрудник Института химической физики РАН.
Эту проблему завершения репликации на концах линейных молекул ДНК
блестяще разобрал и решил российский ученый А.Оловников, ныне
сотрудник Института химической физики РАН.
Он пришел к следующим выводам:
1. Если репликация будет происходить в соответствии с
общепринятой схемой, то в каждом цикле ДНК должна укорачиваться
на длину праймера РНК, т.е. на 10-20 нуклеотидов.
2. Последовательное исчезновение концевых участков в хромосоме
через какое-то число циклов репликации начнет приводить к потере
генов, что в свою очередь должно приводить к патологическим
изменениям в различных структурах и функциях клетки, включая
изменения в хромосомном наборе, ускоренном старении и смерти.
А.Оловников предложил формулу для расчета продолжительности жизни
любого клона клеток in vitro:
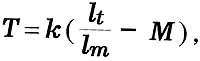
где
Т — срок предстоящей жизни клеток;
k — коэффициент корреляции между сроком жизни клона клеток и
числом репликаций ДНК;
lt - длина теломерного участка;
lm — длина фрагмента ДНК, утрачиваемого в ходе каждого цикла
репликаций;
M — число уже прошедших репликаций.
Именно в этой формуле заключается эффект новизны гипотезы
Оловникова.
3. В качестве защиты генетического материала каждая хромосома
должна обладать двумя специфическими концевыми участками,
расположенными на противоположных концах нити ДНК. Он
предположил, что эти теломерные участки не несут генетической
информации, но выполняют буферную функцию. Именно в них
располагаются концевые праймеры РНК. В ходе каждого цикла
репликации молекула ДНК укорачивается на длину праймера, но
укорачивается неинформативная теломерная часть, и гены,
расположенные в основной части молекулы ДНК, при этом не
страдают.
Работы Оловникова, опубликованные в 1971 году на русском и в 1973
г. на английском языках, оставались незамеченными, в первую
очередь, его западными коллегами, до 1988 года.
Связано это было, видимо, с тем, что теломеру или теломерную ДНК
весьма трудно выделить в чистом виде, поскольку концентрация ее в
геноме обычной клетки чрезвычайно низка.
Прогресс в изучении теломер начался в конце 1970-х — начале
1980-х годов, когда американские генетики Е. Блакберн и Дж. Голл
сумели выделить и расшифровать структуру теломерной ДНК. Эта, как
оказалось, очень простая последовательность нуклеотидов,
присутствует у всех изученных на сегодняшний день организмов, и
все теломерные фрагменты похожи друг на друга. Как правило, это
гекса- или октонуклеотид, обогащенный тимином на 5'конце и
состоящий целиком из гуанина на 3'конце, т.е., например, у
человека это последовательность из нуклеотидов TTAGGG. Теломерный
участок повторен многократно, в результате чего на конце каждой
хромосомы находится блок из одинаковых последовательностей
нуклеотидов, выполняющих буферную функцию в ходе репликации ДНК.
За состоянием этого блока следит особый белок-фермент теломераза,
главной функцией которой является добавление теломерного участка
на конец каждой молекулы ДНК перед каждым циклом репликации.
Оказалось, что теломераза активна не во всех клетках. Она
сохраняет активность в клетках зародышевого пути, т.е. тех, из
которых образуются мужские и женские половые клетки, а при
последующем слиянии которых — новый организм. Наследственный
материал этих клеток должен быть защищен максимально надежно,
поскольку именно по этому пути происходит передача
наследственного материала последующим поколениям, и эти клетки
постоянно делятся. Теломеры в клетках зародышевого пути,
благодаря постоянно высокой активности теломеразы, сохраняют
нормальную длину.
Что касается соматических клеток, то у них есть лимит на число
клеточных делений. Американским ученым Л.Хейфликом в 1965 году
было показано, что если для культивирования взять клетки у
новорожденных детей, они могут пройти 80-90 делений, клетки,
взятые у 70-летних, делятся только 20-30 раз. Ограничение на
число клеточных делений называют барьером Хейфлика. Обычно клетки
не преодолевают барьер из 20-90 делений, по мнению Хейфлика —
50+-10. Оказалось, что теломераза в соматических клетках,
культивируемых in vitro, неактивна, и теломеры постоянно
укорачиваются.
Однако, в раковых клетках, которые также являются соматическими,
клеточные деления не прекращаются, и теломеры у них не
укорачиваются. Оказалось, что почти во всех образцах опухолевых
клеток, взятых как из культуры, так и из целого организма,
активность теломеразы сохраняется на высоком уровне. Это
обстоятельство позволило ученым пофантазировать на следующую
тему: если бы удалось найти химический реагент, избирательно
инактивирующий теломеразу, то при его применении опухолевые
клетки быстро бы достигали барьера Хейфлика и погибали, в то
время как в остальных соматических клетках действие этого агента
не ощущалось бы, т.к. в них теломеразы нет.
Суть последнего эксперимента, взбудоражившего мир, заключается в
следующем. Группе американского исследователя Дж.Шея с помощью
генно-инженерных методов удалось ввести в геном соматических
клеток в системе in vitro, ген теломеразы, снабженный
регулирующими фрагментами ДНК, которые и заставили этот ген
активно работать в тех клетках, в которых он обычно не работает.
Авторы обнаружили, что длина теломер в этих клетках начала
увеличиваться, так же, как и продолжительность жизни клеточных
культур: сверх обычных 50 делений клетки прошли дополнительные 20
делений.
Результат этот несомненно интересен с чисто научной точки зрения,
хотя и не более значителен, чем все остальное, что делалось
раньше в такой интересной области молекулярной генетики, как
изучение организации хромосом и теломер, в частности. Напомним,
что сами авторы оценили свои результаты очень скромно. Каким
будет практическое применение полученных знаний о структуре
теломер на самом деле — покажет время. Предыдущая история
развития генетики многократно показывала, что какими бы смелыми
не были фантазии исследователей, проходило два-три года и новые
эксперименты преподносили еще более ошеломляющие результаты.
Можно их ожидать и теперь. Недаром же общим местом стало
утверждение, что XXI век — это век биологии.
На рисунках:
Рис.1 — ДНК до ведения гена теломеразы.
Рис.2 — после введения гена теломеразы.
стр.
|